Najważniejsze powody:
1. Odpowiednia chemia reakcji
Ołów bardzo dobrze współpracuje z kwasem siarkowym (elektrolitem). Tworzy stabilny i odwracalny układ reakcji chemicznych (ładowanie ↔ rozładowanie), co jest podstawą działania akumulatora. Dzięki temu można go wielokrotnie ładować bez szybkiej degradacji.
2. Wysokie napięcie pojedynczego ogniwa
Reakcja ołowiu z jego tlenkiem daje około 2 V na ogniwo, co jest wygodne w praktyce (np. 12 V = 6 ogniw). Inne materiały często dają niższe napięcia lub są mniej stabilne.
3. Duża odporność na przeciążenia
Ołów dobrze znosi:
- chwilowe duże prądy
- głębsze rozładowania (zwłaszcza w wersji żelowej)
To ważne np. w zasilaniu awaryjnym czy systemach PV.
4. Stabilność i bezpieczeństwo
W porównaniu z bardziej „energetycznymi” metalami (np. litem), ołów jest:
- mniej reaktywny
- bardziej przewidywalny
- mniej podatny na zapłon
Dlatego akumulatory żelowe są uznawane za bezpieczne.
5. Niska cena i dostępność
Ołów jest stosunkowo tani i łatwo dostępny, co sprawia, że takie akumulatory są ekonomiczne.
6. Bardzo dobry recykling
Akumulatory ołowiowe są jednymi z najlepiej recyklingowanych produktów na świecie (ponad 90%). Ołów można odzyskiwać i używać ponownie.
A dlaczego „żelowy”?
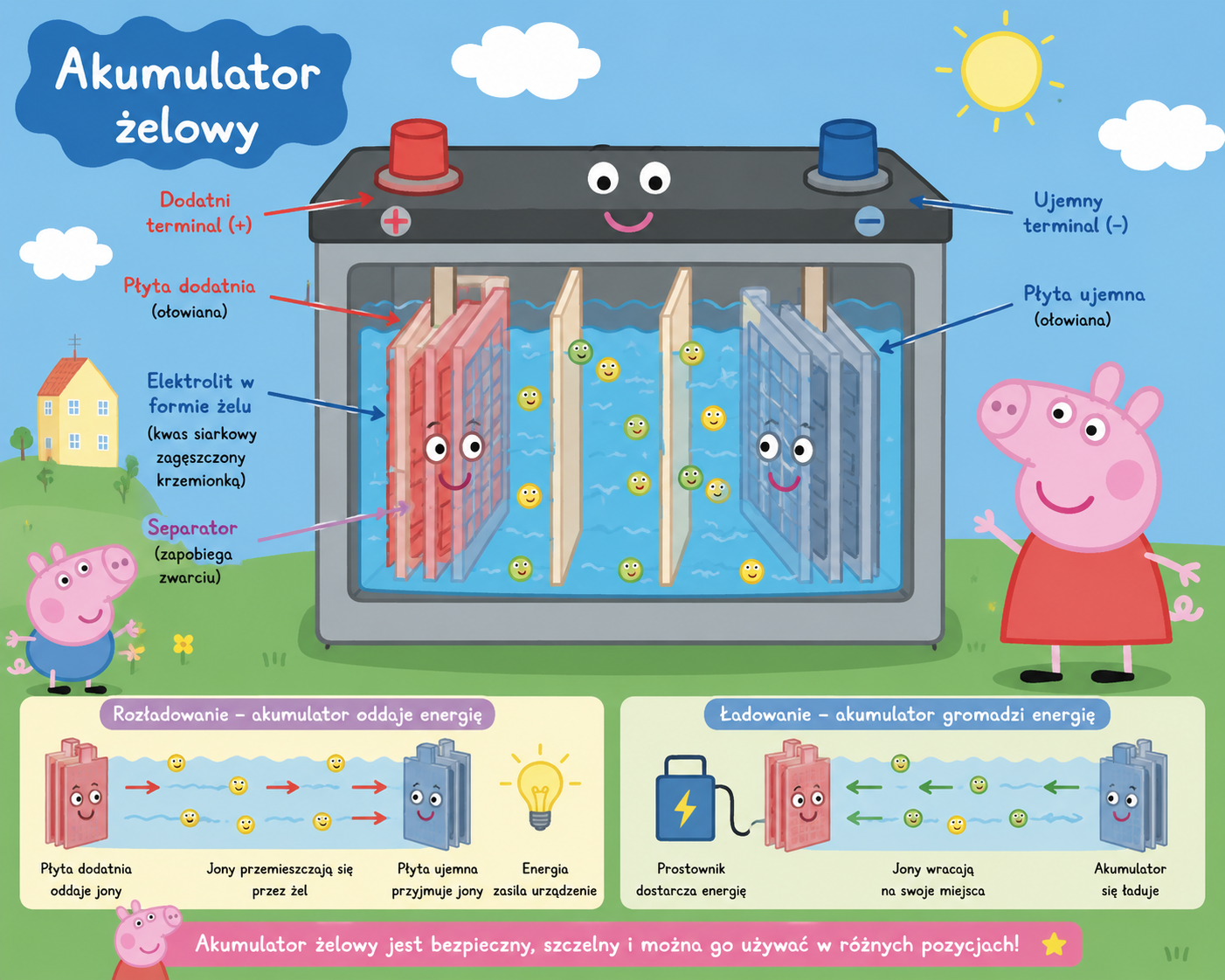
W akumulatorze żelowym elektrolit (kwas siarkowy) jest zagęszczony krzemionką i ma postać żelu. To:
- zmniejsza ryzyko wycieku
- poprawia pracę w różnych pozycjach
- zwiększa odporność na wstrząsy
Ale chemia nadal opiera się na ołowiu — to kluczowy element.



